Halo jagoan sains! Kita sering ngomongin listrik statis, misalnya kenapa sisir plastik bisa menarik sobekan kertas kecil setelah digosok ke rambut. Jawabannya ada di bagian paling kecil dari semua benda di dunia ini: ATOM.
Untuk ngerti kenapa ada “listrik”, kita harus kenalan dulu sama si atom ini. Tapi, gambaran kita tentang atom itu nggak langsung keren kayak sekarang, lho. Para ilmuwan butuh waktu ratusan tahun, seperti detektif yang memecahkan misteri super kecil!
Yuk, kita ikuti perjalanan para “detektif sains” ini!
Perjalanan Mengungkap Wajah Atom
Bayangin atom itu kayak donat. Awalnya orang mikir donat itu cuma bulatan polos, lalu ada yang sadar ada mesesnya, terus ada yang sadar ternyata tengahnya bolong! Kira-kira begitulah evolusi model atom.
1. Model Atom Dalton: Si Bola Biliar (Awal 1800-an)

Detektif pertama kita adalah John Dalton. Menurutnya:
- Atom itu seperti bola biliar atau kelereng. Super kecil, padat, dan pejal.
- Atom itu bagian terkecil yang nggak bisa dibelah-belah lagi.
- Setiap unsur (misalnya emas, oksigen, besi) punya atom yang sama persis.
Analogi gampangnya: Bayangin kamu punya banyak kelereng. Semua kelereng itu utuh dan nggak bisa kamu pecahin lagi. Itulah atom menurut Dalton.
Kelemahannya: Model ini belum bisa menjelaskan tentang kelistrikan. Kalau atom cuma bola netral, dari mana datangnya muatan positif dan negatif? Misteri berlanjut!
2. Model Atom Thomson: Si Roti Kismis (Sekitar tahun 1904)

Detektif kedua, J.J. Thomson, bikin penemuan heboh: ia menemukan elektron, partikel super kecil yang bermuatan negatif (-). Gara-gara ini, gambaran atom pun berubah!
- Menurut Thomson, atom itu seperti bola yang bermuatan positif.
- Di dalam bola positif itu, tersebar elektron-elektron negatif, kayak kismis di dalam roti.
- Jumlah muatan positif dan negatifnya sama, jadi atom itu netral.
Analogi gampangnya: Bayangin onde-onde. Adonan kuenya itu bola positif, dan biji wijen yang nempel di permukaannya adalah elektron-elektron negatif.
Kelebihannya: Model ini sudah bisa menjelaskan adanya partikel bermuatan dalam atom. Kita mulai dekat dengan jawaban soal listrik!
3. Model Atom Rutherford: Si Tata Surya Mini (Tahun 1911)

Detektif Ernest Rutherford penasaran sama “roti kismis”-nya Thomson. Dia melakukan percobaan super keren dengan menembakkan partikel ke lempengan emas super tipis. Hasilnya mengejutkan!
- Kebanyakan partikelnya tembus! Ini berarti atom itu sebagian besar adalah ruang kosong.
- Ada sedikit partikel yang memantul balik. Ini berarti muatan positif tidak tersebar, tapi berkumpul di tengah dalam bagian yang sangat kecil, padat, dan berat. Bagian ini ia namakan inti atom (nukleus).
- Elektron-elektron negatif ternyata mengelilingi inti atom dari jarak yang jauh, mirip seperti planet mengelilingi matahari.
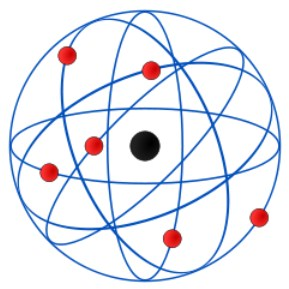
Analogi gampangnya: Bayangin sebuah tata surya mini. Matahari adalah inti atom (positif), dan planet-planet yang mengorbit adalah elektron (negatif).
Kelemahannya: Kalau elektron terus-terusan mengelilingi inti, lama-lama energinya habis dong dan bisa “jatuh” ke inti. Tapi kok kenyataannya atom itu stabil?
4. Model Atom Bohr: Si Lintasan Berlapis (Tahun 1913)
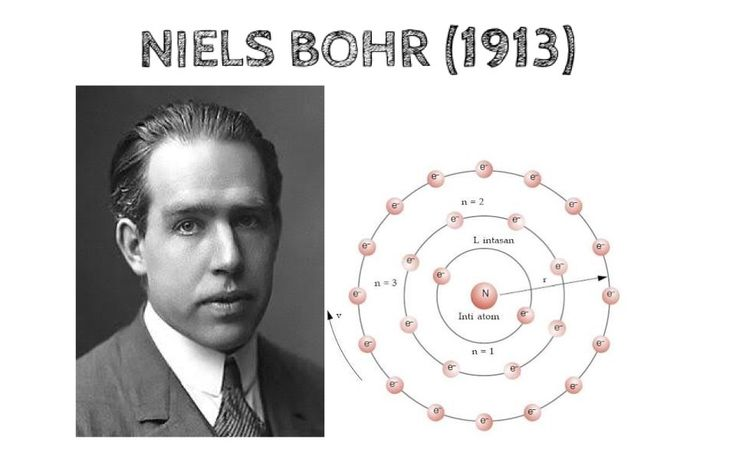
Niels Bohr, muridnya Rutherford, datang memperbaiki model gurunya.
- Elektron memang mengelilingi inti atom, tapi tidak di sembarang tempat.
- Elektron hanya boleh berada di lintasan-lintasan khusus yang disebut kulit atom. Setiap kulit punya tingkat energi tertentu.
- Elektron bisa pindah (loncat) dari kulit satu ke kulit lain, tapi tidak bisa berada di antara dua kulit.
Analogi gampangnya: Bayangin penonton di stadion sepak bola. Mereka hanya bisa duduk di baris kursi yang sudah ada (kulit 1, kulit 2, dst). Mereka tidak bisa duduk melayang di antara dua baris.
Koneksi ke Listrik Statis: Nah, di sinilah kuncinya! Elektron yang berada di kulit paling luar adalah yang paling gampang lepas atau ditarik oleh atom lain. Peristiwa lepas-tangkapnya elektron terluar inilah yang menyebabkan fenomena listrik statis!
5. Model Atom Modern: Si Awan Kabut (Sejak 1920-an)
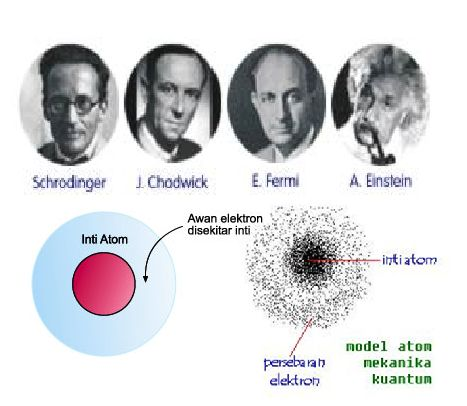
Para ilmuwan seperti Schrödinger dan Heisenberg menyempurnakan model Bohr.
- Posisi elektron itu tidak bisa dipastikan 100% seperti planet di lintasan.
- Kita hanya bisa menentukan daerah kemungkinan terbesar untuk menemukan elektron. Daerah ini disebut awan elektron atau orbital.
- Semakin tebal “awan”-nya di suatu titik, semakin besar kemungkinan elektron ada di sana.
Analogi gampangnya: Bayangin kipas angin yang menyala kencang. Kamu tahu baling-balingnya ada di dalam area yang berputar itu, tapi kamu tidak bisa menunjuk dengan pasti di mana posisi satu baling-baling pada waktu tertentu. Area berputar yang buram itulah “awan elektron”.
Kesimpulan Keren & Hubungannya dengan Listrik Statis
- Dalton: Atom itu bola pejal.
- Thomson: Atom itu roti kismis (ada elektronnya).
- Rutherford: Atom punya inti di tengah & elektron mengelilingi (tata surya mini).
- Bohr: Elektron punya lintasan/kulit khusus.
- Modern: Posisi elektron ada di dalam “awan” kemungkinan.
Jadi, kenapa sisir bisa menarik kertas? Karena saat sisir digosok ke rambut, elektron dari kulit terluar atom di rambutmu pindah ke sisir. Sisir jadi kelebihan elektron (bermuatan negatif). Saat didekatkan ke kertas yang netral, sisir ini bisa menarik muatan positif di kertas.
Keren, kan? Dengan memahami evolusi model atom, kita jadi tahu “biang kerok” di balik fenomena listrik statis, yaitu si elektron yang suka loncat-loncat!


